Química Básica
Escuela de Química
Facultad de Ciencias
Universidad Industrial de Santander
Módulo 3. Enlace químico, soluciones y estequiometría.
Lección 3.2 Soluciones.
Volver al módulo

1. Preparación de la lección
Competencias de la lección
- Definir soluciones y clasificar sus tipos según el estado físico de sus componentes: Comprender qué es una solución y diferenciar entre tipos de soluciones en función del estado físico de sus componentes (sólido, líquido o gas).
- Analizar el concepto de solubilidad y los tipos de soluciones según la cantidad de soluto: Explicar qué es la solubilidad y la miscibilidad, y clasificar las soluciones como saturadas, insaturadas o sobresaturadas, describiendo factores que afectan la solubilidad y la velocidad de disolución.
- Comprender y calcular la concentración de una solución en diferentes unidades: Definir la concentración y utilizar diversas unidades de medida como porcentaje en masa (%m/m), masa-volumen (%m/v), volumen-volumen (%v/v), molaridad, molalidad, partes por millón, partes por billón y fracción molar; realizar conversiones entre estas unidades.
- Aplicar el concepto de dilución para ajustar la concentración de soluciones: Calcular la dilución de soluciones y comprender cómo las concentraciones cambian con la adición de solventes.
- Distinguir entre electrolitos y no electrolitos: Diferenciar soluciones que contienen electrolitos de aquellas con no electrolitos, y entender la importancia de esta distinción en conductividad y propiedades de las soluciones.
Catálogo de Videos
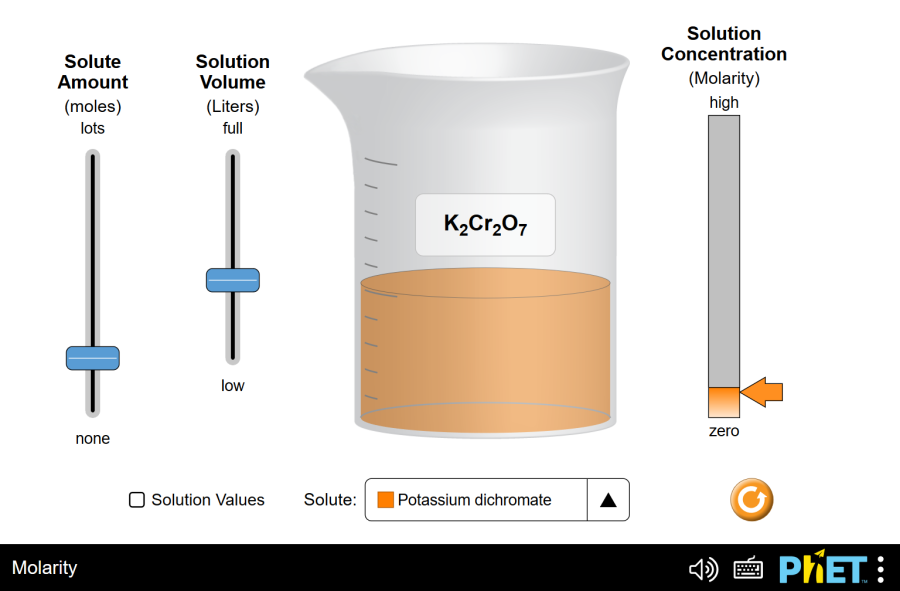
Catálogo de Simuladores
Catálogo de Libros
2. Profundización de la lección
- (T11.1) Definición de soluciones: Definición de soluciones; Tipos de soluciones según el estado físico de sus componentes. (Bibliografía: Whitten p.506, Rosenberg p.197, Chang p.519)
- (T11.2) Solubilidad: Concepto de solubilidad y miscibilidad; Tipos de soluciones según la cantidad de soluto disuelto: soluciones saturadas, insaturadas y sobresaturadas; Factores que afectan la solubilidad y la velocidad de disolución. (Bibliografía: Whitten p.510, Brown p.518, Whitten p.513, Rosenberg p.225, Brown p.520, Rosenberg p.22)
- (T11.3) Concentración de una solución y tipos de unidades de concentración: Concepto de concentración; Porcentaje en masa (%m/m); porcentaje en masa-volumen (%m/v); porcentaje en volumen (%v/v); Molaridad; Molalidad; partes por millón; partes por billón; fracción molar; Interconversión de unidades de concentración: concepto de base de cálculo. (Bibliografía: Rosenberg p.197, Rosenberg p.200, Whitten p.516, Brown p.400, Whitten p.517, Rosenberg p.226)
- (T11.4) Dilución de las soluciones: Dilución de las soluciones; *Concepto de electrolitos y no electrolitos. (Bibliografía: Brown p.141, Whitten p.102, Rosenberg p.200, Brown p.126, Whitten p.527)
Lección 3.2 Soluciones.
3. Reto de la lección
Resumen
4. Cierre de la lección
Autoevaluación
¿Qué es una solución y cómo se clasifican según el estado físico de sus componentes?
¿Qué factores afectan la solubilidad y la velocidad de disolución de un soluto en un solvente?
¿Cuál es la diferencia entre soluciones saturadas, insaturadas y sobresaturadas?
¿Cuáles son las principales unidades de concentración de una solución y en qué contextos se utilizan cada
una de ellas?
¿Qué es una dilución y cómo se diferencian los electrolitos de los no electrolitos en soluciones diluidas?